Saiki, telung obat terapi gen wis disetujoni kanggo pemasaran, yaiku: (1) Ing tanggal 21 Juli 2022, PTC Therapeutics, Inc. (NASDAQ: PTCT) ngumumake yen terapi gen AAV Upstaza™ disetujoni dening Komisi Eropa Iku terapi gen pertama sing dipasarake langsung menyang otak (deleng artikel sadurunge: Tonggak sejarah liyane ing terapi gen ing donya sing disetujoni langsung ing AV Therapy Therapy)(2) Tanggal 17 Agustus 2022, US Food and Drug Administration (FDA) nyetujoni terapi gen Bluebird Bio Zynteglo (betibeglogene autotemcel, beti-cel) kanggo perawatan talasemia beta.Persetujuan terapi ing Amerika Serikat mesthine minangka "bantuan ing salju" kanggo Bluebird Bio, sing ana ing krisis finansial.(3) Ing tanggal 24 Agustus 2022, BioMarin Pharmaceutical (BioMarin) ngumumake yen Komisi Eropa nyetujoni pemasaran bersyarat ROCTAVIAN™ (valoctocogene roxaparvovec), terapi gen kanggo hemofilia A, kanggo perawatan pasien sing ora duwe riwayat inhibitor faktor FVIII lan antibodi AAV5 negatif pasien diwasa karo Hemofilia Hemofilia sing disetujoni sadurunge.Nganti saiki, 41 obat terapi gen wis disetujoni kanggo pemasaran ing saindenging jagad.
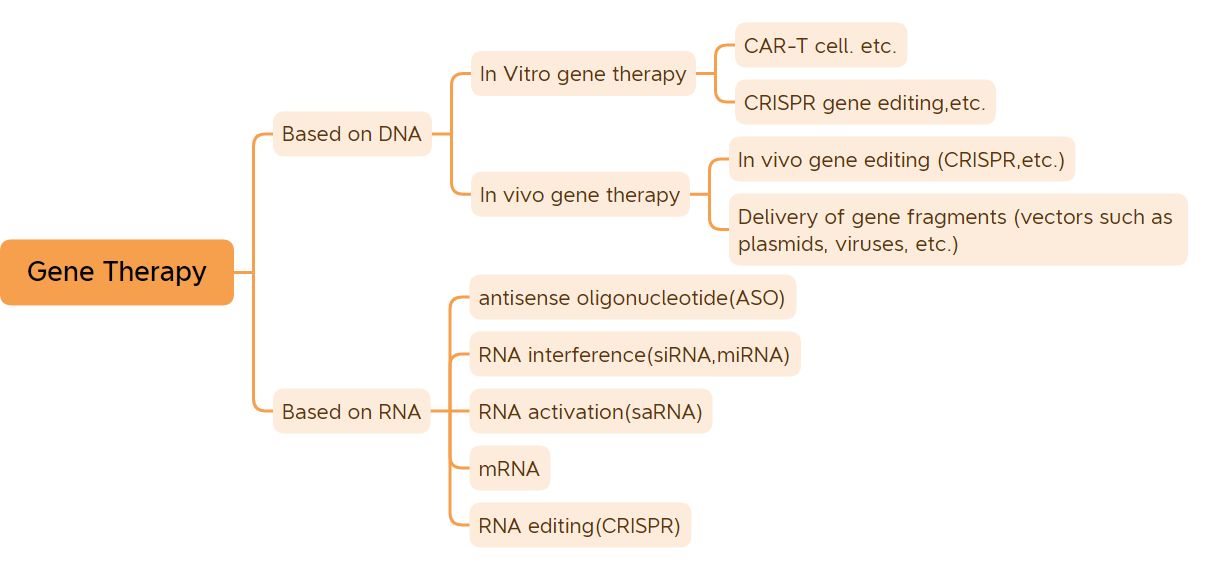
Gen minangka unit genetik dhasar sing ngontrol sipat.Kejaba gen saka sawetara virus, sing kasusun saka RNA, gen paling organisme dumadi saka DNA.Umume penyakit ing organisme disebabake interaksi antarane gen lan lingkungan, lan akeh penyakit sing bisa ditambani utawa dikurangi kanthi cara terapi gen.Terapi gen dianggep minangka revolusi ing bidang kedokteran lan farmasi.Obat terapi gen sing amba kalebu obat adhedhasar obat DNA sing dimodifikasi DNA (kayata obat terapi gen in vivo berbasis vektor virus, obat terapi gen in vitro, obat plasmid telanjang, lan liya-liyane) lan obat RNA (kayata obat oligonukleotida antisense, obat siRNA, lan terapi gen mRNA, lsp.);Obat terapi gen sing ditetepake utamane kalebu obat DNA plasmid, obat terapi gen adhedhasar vektor virus, obat terapi gen adhedhasar vektor bakteri, sistem panyuntingan gen lan obat terapi sel sing diowahi sacara genetis in vitro.Sawise pirang-pirang taun pembangunan sing tortuous, obat terapi gen wis entuk asil klinis sing nyenengake.(ora kalebu vaksin DNA lan vaksin mRNA), 41 obat terapi gen wis disetujoni kanggo marketing ing donya.Kanthi diluncurake produk lan pangembangan teknologi terapi gen kanthi cepet, terapi gen bakal diwiwiti kanthi cepet.
Klasifikasi terapi gen (Sumber gambar: Biological Jingwei)
Artikel iki nyathet 41 terapi gen sing wis disetujoni kanggo marketing (ora kalebu vaksin DNA lan vaksin mRNA).
1. Terapi gen in vitro
(1) Strimvelis
Perusahaan: Dikembangake dening GlaxoSmithKline (GSK).
Wektu kanggo pasar: Disetujui dening Uni Eropa ing Mei 2016.
Indikasi: Kanggo perawatan saka immunodeficiency gabungan abot (SCID).
Cathetan: Proses umum terapi iki yaiku njupuk sel stem hematopoietik pasien dhewe, ngembangake lan kultur in vitro, banjur nggunakake retrovirus kanggo ngenalake salinan gen ADA (adenosine deaminase) fungsional menyang sel stem hematopoietik, lan pungkasane nransfer sel stem hematopoietik sing dimodifikasi.Sel stem hematopoietik dilebokake maneh menyang awak.Asil klinis nuduhake yen tingkat kaslametan 3 taun pasien ADA-SCID sing diobati karo Strimvelis yaiku 100%.
(2) Zalmoxis
Perusahaan: Diprodhuksi dening MolMed, Italia.
Wektu kanggo pasar: Entuk wewenang pemasaran bersyarat EU ing 2016.
Indikasi: Digunakake kanggo terapi adjuvant sistem kekebalan pasien sawise transplantasi sel stem hematopoietik.
Cathetan: Zalmoxis minangka imunoterapi gen bunuh diri sel T alogenik sing dimodifikasi dening vektor retroviral.Gen bunuh diri 1NGFR lan HSV-TK Mut2 ngidini wong nggunakake ganciclovir sawayah-wayah kanggo mateni sel T sing nyebabake respon imun sing ora becik, nyegah kerusakan luwih lanjut saka GVHD sing bisa kedadeyan, lan mulihake fungsi kekebalan ing pasien kanthi HSCT haploidentical sawise operasi Escort.
(3) Invossa-K
Perusahaan: Dikembangake dening perusahaan TissueGene (KolonTissueGene).
Wektu kanggo pasar: Disetujui kanggo listing ing Korea Selatan ing Juli 2017.
Indikasi: Kanggo perawatan atritis lutut degeneratif.
Cathetan: Invossa-K minangka terapi gen sel alogenik sing nglibatake kondrosit manungsa.Sèl alogenik diowahi sacara genetis ing vitro, lan sel sing diowahi bisa ngekspresikan lan mbebasake faktor pertumbuhan transformasi β1 (TGF-β1) sawise injeksi intra-artikular.β1), saéngga ningkatake gejala osteoarthritis.Asil klinis nuduhake yen Invossa-K bisa ningkatake arthritis lutut kanthi signifikan.Lisensi kasebut dicabut dening regulator obat Korea Selatan ing taun 2019 amarga pabrikan salah menehi label bahan sing digunakake.
(4) Zynteglo
Perusahaan: Dikembangake dening perusahaan bio bluebird Amerika (bluebird bio).
Wektu kanggo pasar: Disetujui dening Uni Eropa ing 2019, lan disetujoni dening FDA ing Agustus 2022.
Indikasi: Kanggo perawatan saka β-thalassemia gumantung transfusi.
Cathetan: Zynteglo minangka terapi gen lentiviral in vitro, sing nggunakake vektor lentiviral kanggo ngenalake salinan fungsional gen β-globin normal (gen βA-T87Q-globin) menyang sel stem hematopoietik sing dibuang saka pasien., banjur infus sel stem hematopoietik autologous sing diowahi sacara genetis iki bali menyang pasien.Sawise pasien duwe gen βA-T87Q-globin normal, dheweke bisa ngasilake protein HbAT87Q normal, sing bisa nyuda utawa ngilangi kabutuhan transfusi getih kanthi efektif.Iki minangka terapi siji-wektu sing dirancang kanggo ngganti transfusi getih seumur hidup lan obat seumur hidup kanggo pasien umur 12 taun lan luwih lawas.
(5) Skysona
Perusahaan: Dikembangake dening perusahaan bio bluebird Amerika (bluebird bio).
Wektu kanggo pasar: Disetujui dening EU kanggo marketing ing Juli 2021.
Indikasi: Kanggo perawatan awal adrenoleukodystrophy serebral (CALD).
Cathetan: Terapi gen Skysona minangka terapi gen siji-sijine sing disetujoni kanggo perawatan awal adrenoleukodystrophy serebral (CALD).Skysona (elivaldogene autotemcel, Lenti-D) minangka lentiviral sel induk hematopoietik in vitro terapi gen Lenti-D.Proses umum terapi kasebut kaya ing ngisor iki: sel stem hematopoietik autologous dijupuk saka pasien, diowahi in vitro dening lentivirus sing nggawa gen ABCD1 manungsa, lan banjur diinfus maneh menyang pasien.Kanggo perawatan pasien ing umur 18 taun kanthi mutasi gen ABCD1 lan CALD.
(6) Kymria
Perusahaan: Dikembangake dening Novartis.
Wektu kanggo pasar: Disetujui dening FDA ing Agustus 2017.
Indikasi: Perawatan saka leukemia limfoblastik akut sel B prekursor (ALL) lan DLBCL kambuh lan refrakter.
Cathetan: Kymriah minangka obat terapi gen in vitro lentiviral, terapi CAR-T pisanan sing disetujoni ing donya, ngarahake CD19 lan nggunakake faktor co-stimulatory 4-1BB.Rega $475,000 ing AS lan $313,000 ing Jepang.
(7) Wis
Perusahaan: Dikembangake dening Kite Pharma, anak perusahaan Gilead.
Wektu kanggo pasar: Disetujui dening FDA ing Oktober 2017.
Indikasi: Kanggo perawatan limfoma sel B gedhe sing kambuh utawa refraktori.
Cathetan: Yescarta minangka terapi gen retroviral in vitro.Iki minangka terapi CAR-T nomer loro sing disetujoni ing saindenging jagad.Target CD19 lan nggunakake faktor kostimulasi CD28.Rega ing AS yaiku $ 373.000.
(8) Tekartus
Perusahaan: Dikembangake dening Gilead (GILD).
Wektu kanggo pasar: Disetujui dening FDA ing Juli 2020.
Indikasi: Kanggo limfoma sel mantel kambuh utawa refrakter.
Cathetan: Tecartus minangka terapi sel CAR-T autologous sing nargetake CD19, lan minangka terapi CAR-T katelu sing disetujoni kanggo marketing ing donya.
(9) Breyanzi
Perusahaan: Dikembangaké déning Bristol-Myers Squibb (BMS).
Wektu kanggo pasar: Disetujui dening FDA ing Februari 2021.
Indikasi: Limfoma sel B gedhe (LBCL) kambuh utawa refraktori (R/R).
Cathetan: Breyanzi minangka terapi gen in vitro adhedhasar lentivirus, lan terapi CAR-T kaping papat sing disetujoni kanggo marketing ing donya, ngarahake CD19.Persetujuan Breyanzi minangka tonggak sejarah kanggo Bristol-Myers Squibb ing bidang imunoterapi seluler, sing dipikolehi Bristol-Myers nalika entuk Celgene kanthi rega $ 74 milyar ing taun 2019.
(10) Abekma
Perusahaan: Dikembangake bebarengan dening Bristol-Myers Squibb (BMS) lan bio bluebird.
Wektu kanggo pasar: Disetujui dening FDA ing Maret 2021.
Indikasi: Multiple myeloma kambuh utawa refrakter.
Cathetan: Abecma minangka terapi gen in vitro adhedhasar lentivirus, terapi sel CAR-T pisanan ing donya sing nargetake BCMA, lan terapi CAR-T kaping lima sing disetujoni dening FDA.Prinsip obat yaiku kanggo nyebut reseptor BCMA chimeric ing sel T autologous pasien liwat modifikasi genetik sing dimediasi lentivirus in vitro.Sadurunge infus obat gen sel, pasien nampa rong senyawa cyclophosphamide lan fludarabine kanggo pre-treatment.Perawatan kanggo mbusak sel T sing ora diowahi saka pasien, lan banjur nglebokake sel T sing dimodifikasi maneh menyang awak pasien kanggo nggoleki lan mateni sel kanker sing nyatakake BCMA.
(11) Libmeldy
Perusahaan: Dikembangake dening Orchard Therapeutics.
Wektu menyang pasar: Disetujui dening Uni Eropa kanggo listing ing Desember 2020.
Indikasi: Kanggo perawatan leukodistrofi metachromatic (MLD).
Cathetan: Libmeldy minangka terapi gen adhedhasar modifikasi gen lentiviral in vitro saka sel CD34+ autologous.Data klinis nuduhake yen infus intravena Libmeldy siji efektif kanggo ngowahi dalan MLD awal lan gangguan motorik lan kognitif sing abot ing pasien sing ora diobati ing umur sing padha.
(12) Benodha
Perusahaan: Dikembangake dening WuXi Junuo.
Wektu menyang pasar: Disetujoni kanthi resmi dening NMPA ing September 2021.
Indikasi: Perawatan limfoma sel B gedhe sing kambuh utawa refraktori (r / r LBCL) ing pasien diwasa sawise terapi sistemik baris kapindho utawa luwih.
Cathetan: Benoda minangka terapi gen anti-CD19 CAR-T, lan uga minangka produk inti saka WuXi Junuo.Iki minangka produk CAR-T nomer loro sing disetujoni ing China, kajaba limfoma sel B gedhe sing kambuh / refraktori.Kajaba iku, WuXi Junuo uga ngrancang ngembangake injeksi Ruiki Orenza kanggo perawatan macem-macem indikasi liyane, kalebu limfoma folikel (FL), limfoma sel mantel (MCL), leukemia limfositik kronis (CLL), limfoma sel B gedhe (DLBCL) lan leukemia limfoblastik akut (ALL).
(13) CARVIKTI
Perusahaan: produk pisanan sing disetujoni Legenda Bio.
Wektu kanggo pasar: Disetujui dening FDA ing Februari 2022.
Indikasi: Perawatan myeloma multipel kambuh utawa refraktori (R/R MM).
Cathetan: CARVYKTI (ciltacabtagene autoleucel, diarani Cilta-cel) minangka terapi gen imun sel CAR-T kanthi rong antibodi domain siji sing ngarahake antigen maturasi sel B (BCMA).Data kasebut nuduhake yen CARVYKTI nuduhake tingkat respon sakabèhé nganti 98% ing pasien karo myeloma multipel kambuh utawa refraktori sing wis nampa papat utawa luwih terapi sadurunge, kalebu inhibitor proteasome, imunomodulator, lan antibodi monoklonal anti-CD38.
2. Terapi gen in vivo adhedhasar vektor virus
(1) Gendicine / lair maneh
Company: Dikembangaké dening Shenzhen Saibainuo Company.
Wektu kanggo pasar: Disetujui kanggo listing ing China ing 2003.
Indikasi: Kanggo perawatan karsinoma sel skuamosa ing sirah lan gulu.
Cathetan: injeksi adenovirus p53 manungsa rekombinan Gendicine / Jinshengsheng minangka obat terapi gen vektor adenovirus kanthi hak properti intelektual sing diduweni dening Perusahaan Shenzhen Saibainuo.Obat kasebut kasusun saka gene suppressor tumor manungsa normal p53 lan rekombinan rekombinan sing dimodifikasi kanthi artifisial Human adenovirus tipe 5 kasusun saka jinis adenovirus manungsa 5. Tilas minangka struktur utama obat kanggo ngleksanakake efek anti-tumor, lan sing terakhir utamane minangka operator.Vektor adenovirus nggawa gen terapeutik p53 menyang sel target, lan nuduhake gen penekan tumor p53 ing sel target.Produk kasebut bisa ngatur macem-macem gen anti-kanker lan mudhun-ngatur aktivitas macem-macem onkogen, saéngga nambah efek anti-tumor awak lan entuk tujuan mateni tumor.
(2) Rigvir
Perusahaan: Dikembangake dening perusahaan Latvia Latima.
Wektu kanggo pasar: Disetujui ing Latvia ing 2004.
Indikasi: Kanggo perawatan melanoma.
Cathetan: Rigvir minangka terapi gen adhedhasar vektor enterovirus ECHO-7 sing diowahi gen, sing wis digunakake ing Latvia, Estonia, Polandia, Armenia, Belarus lan papan liyane, lan uga didaftar ing EMA Uni Eropa..Kasus klinis sajrone sepuluh taun kepungkur wis mbuktekake manawa virus oncolytic Rigvir aman lan efektif, lan bisa ningkatake tingkat kaslametan pasien melanoma kanthi kaping 4-6.Kajaba iku, terapi kasebut uga cocog kanggo macem-macem kanker liyane, kalebu kanker kolorektal, kanker pankreas, kanker kandung kemih.kanker, kanker ginjel, kanker prostat, kanker paru-paru, kanker uterus, lymphosarcoma, etc.
(3) Oncorine/Ankerui
Perusahaan: Dikembangake dening Shanghai Sunway Biotechnology Co., Ltd.
Wektu kanggo pasar: Disetujui kanggo listing ing China ing 2005.
Indikasi: Perawatan tumor sirah lan gulu, kanker ati, kanker pankreas, kanker serviks lan kanker liyane.
Cathetan: Oncorine minangka produk terapi gen virus oncolytic nggunakake adenovirus minangka vektor.Adenovirus oncolytic sing dipikolehi bisa niru khusus ing tumor sing kurang utawa gen p53 sing ora normal, nyebabake lisis sel tumor, saengga bisa mateni sel tumor.tanpa ngrusak sel normal.Asil klinis nuduhake yen Anke Rui nduweni safety lan khasiat sing apik kanggo macem-macem tumor ganas.
(4) Glybera
Perusahaan: Dikembangake dening uniQure.
Wektu kanggo pasar: Disetujui ing Eropa ing 2012.
Indikasi: Perawatan kekurangan lipoprotein lipase (LPLD) kanthi episode pankreatitis sing abot utawa berulang sanajan diet lemak sing diwatesi.
Cathetan: Glybera (alipogene tiparvovec) minangka obat terapi gen adhedhasar AAV minangka vektor.Terapi iki nggunakake AAV minangka vektor kanggo nransfer LPL gene terapi menyang sel otot, supaya sel sing cocog bisa ngasilake jumlah lipoprotein lipase tartamtu, Iki nduweni peran kanggo ngilangi penyakit, lan terapi iki efektif kanggo wektu sing suwe sawise siji administrasi (efek bisa bertahan nganti pirang-pirang taun).Obat kasebut dibuwang ing 2017, lan alasan kanggo ngilangi dhaptar kasebut bisa uga ana gandhengane karo rong faktor: rega sing dhuwur banget lan permintaan pasar sing winates.Biaya rata-rata perawatan siji obat kasebut nganti 1 yuta dolar AS, lan mung siji pasien sing wis tuku lan nggunakake nganti saiki.Sanajan perusahaan asuransi medis mbayar maneh 900.000 dolar AS, nanging uga dadi beban gedhe kanggo perusahaan asuransi kasebut.Kajaba iku, indikasi kanggo obat kasebut arang banget, kanthi tingkat insiden sekitar 1 ing 1 yuta lan tingkat misdiagnosis sing dhuwur.
(5) Imlygic
Perusahaan: Dikembangaké déning Amgen.
Wektu kanggo pasar: Ing 2015, disetujoni kanggo listing ing Amerika Serikat lan Uni Eropa.
Indikasi: Perawatan lesi melanoma sing ora bisa diilangi kanthi operasi.
Cathetan: Imlygic minangka gen sing diowahi sacara genetis (mbusak fragmen gen ICP34.5 lan ICP47, lan nglebokake gen GM-CSF faktor stimulasi koloni granulosit-makrofag manungsa menyang virus) virus oncolytic herpes simplex tipe 1 (HSV-1), terapi virus oncolytic sing disetujoni FDA pisanan.Cara administrasi yaiku injeksi intralesi.Injeksi langsung menyang lesi melanoma bisa nyebabake pecah sel tumor lan ngeculake antigen sing asale saka tumor lan GM-CSF kanggo ningkatake respon imun anti-tumor.
(6) Luxturna
Perusahaan: Dikembangake dening Spark Therapeutics, anak perusahaan Roche.
Wektu kanggo pasar: Disetujui dening FDA ing 2017, lan banjur disetujoni kanggo marketing ing Eropah ing 2018.
Indikasi: Kanggo perawatan bocah lan wong diwasa kanthi mundhut sesanti amarga mutasi ing salinan ganda saka gen RPE65 nanging kanthi jumlah sel retina sing cukup.
Cathetan: Luxturna minangka terapi gen adhedhasar AAV sing diwenehake kanthi injeksi subretinal.Terapi gen nggunakake AAV2 minangka operator kanggo ngenalake salinan fungsional saka gen RPE65 normal menyang sel retina pasien, supaya sel sing cocog nyatakake protein RPE65 normal kanggo ngimbangi cacat protein RPE65 pasien, saéngga bisa nambah visi pasien.
(7) Zolgensma
Perusahaan: Dikembangake dening AveXis, anak perusahaan Novartis.
Wektu kanggo pasar: Disetujui dening FDA ing Mei 2019.
Indikasi: Perawatan atrofi otot balung mburi (Spinal Muscular Atrophy, SMA) pasien ing umur 2 taun.
Cathetan: Zolgensma minangka terapi gen adhedhasar vektor AAV.Obat iki mung siji-wektu rencana perawatan kanggo atrofi otot balung mburi disetujoni kanggo marketing ing donya.kaca, minangka kemajuan tonggak sejarah.Terapi gen iki nggunakake vektor scAAV9 kanggo ngenalake gen SMN1 normal menyang pasien liwat infus intravena, ngasilake protein SMN1 normal, saéngga ningkatake fungsi sel sing kena pengaruh kayata neuron motorik.Ing kontras, obat SMA Spinraza lan Evrysdi mbutuhake dosis bola-bali sajrone wektu sing suwe, kanthi Spinraza diwenehake minangka injeksi spinal saben patang wulan, lan Evrysdi, obat lisan saben dina.
(8) Delytact
Perusahaan: Dikembangake dening Daiichi Sankyo Company Limited (TYO: 4568).
Wektu menyang pasar: Persetujuan bersyarat saka Kementerian Kesehatan, Tenaga Kerja lan Kesejahteraan Jepang (MHLW) ing wulan Juni 2021.
Indikasi: Kanggo perawatan glioma ganas.
Cathetan: Delytact minangka produk terapi gen virus oncolytic kaping papat sing disetujoni sacara global lan produk virus oncolytic pisanan sing disetujoni kanggo perawatan glioma ganas.Delytact minangka virus oncolytic herpes simplex tipe 1 (HSV-1) sing direkayasa sacara genetis sing dikembangake dening Dr. Todo lan kanca-kancane.Delytact ngenalake mutasi pambusakan tambahan menyang génom G207 saka HSV-1 generasi kapindho, nambah réplikasi selektif ing sel kanker lan induksi respon imun anti-tumor, nalika njaga profil safety sing dhuwur.Delytact minangka HSV-1 onkolitik generasi katelu pisanan sing saiki ana ing evaluasi klinis.Persetujuan Delytact ing Jepang adhedhasar uji klinis Fase 2 lengen siji.Ing pasien kanthi glioblastoma berulang, Delytact ketemu titik pungkasan utama kanggo urip setaun, lan asil nuduhake yen Delytact nindakake luwih apik tinimbang G207.Replikasi sing kuat lan aktivitas antitumor sing luwih dhuwur.Iki efektif ing model tumor padhet kalebu payudara, prostat, schwannoma, nasopharyngeal, hepatoseluler, kolorektal, tumor sarung saraf perifer ganas lan kanker tiroid.
(9) Sugih
Perusahaan: Dikembangake dening PTC Therapeutics, Inc. (NASDAQ: PTCT).
Wektu menyang pasar: Disetujui dening EU ing Juli 2022.
Indikasi: Kanggo kekurangan asam L-amino decarboxylase (AADC) aromatik, disetujoni kanggo perawatan pasien umur 18 wulan lan luwih lawas.
Cathetan: Upstaza™ (eladocagene exuparvovec) minangka terapi gen in vivo nggunakake jinis virus adeno-associated 2 (AAV2) minangka vektor.Pasien lara amarga mutasi gen sing ngode enzim AADC.AAV2 nggawa gen sehat sing ngode enzim AADC.Efek terapeutik digayuh kanthi bentuk kompensasi genetik.Ing teori, dosis siji efektif kanggo dangu.Iki minangka terapi gen pertama sing dipasarake langsung menyang otak.Wewenang marketing ditrapake kanggo kabeh 27 negara anggota EU, uga Iceland, Norwegia lan Liechtenstein.
(9) Roktaviani
Perusahaan: Dikembangake dening BioMarin Pharmaceutical (BioMarin).
Wektu menyang pasar: Disetujui dening EU ing Agustus 2022.
Indikasi: Kanggo perawatan pasien diwasa kanthi hemofilia A parah tanpa riwayat inhibisi faktor FVIII lan antibodi AAV5 negatif.
Cathetan: Roctavian (valoctocogene roxaparvovec) nggunakake AAV5 minangka vektor lan nggunakake HLP promotor khusus ati manungsa kanggo nyopir ekspresi faktor koagulasi manungsa wolung (FVIII) kanthi domain B dibusak.Kaputusan Komisi Eropa kanggo nyetujoni pemasaran valoctocogene roxaparvovec adhedhasar data sakabèhé program pangembangan klinis obat kasebut.Antarane wong-wong mau, uji klinis fase III GENEr8-1 nuduhake yen dibandhingake karo data taun sadurunge enrollment, sawise infus siji saka valoctocogene roxaparvovec, Subyek duwe tingkat perdarahan taunan sing luwih murah (ABR), kurang nggunakake preparat protein faktor rekombinan VIII (F8), utawa peningkatan aktivitas F8 sing signifikan ing awak.Sawise perawatan 4 minggu, panggunaan F8 taunan lan ABR sing mbutuhake perawatan dikurangi 99% lan 84%, bedane sacara statistik (p<0.001).Profil safety apik, kanthi ora ana subyek sing ngalami inhibisi faktor F8, ganas, utawa efek samping trombotik, lan ora ana efek samping serius (SAE) sing gegandhengan karo perawatan.
3. Obat-obatan asam nukleat cilik
(1) Vitravene
Perusahaan: dikembangake bebarengan dening Ionis Pharma (biyen Isis Pharma) lan Novartis.
Wektu kanggo pasar: Disetujui dening FDA lan EU EMA ing 1998 lan 1999.
Indikasi: Kanggo perawatan retinitis cytomegalovirus ing pasien HIV-positif.
Cathetan: Vitravene minangka obat oligonukleotida antisense lan obat oligonukleotida pisanan sing disetujoni kanggo marketing ing donya.Ing wiwitan pasar, panjaluk pasar kanggo obat anti-cytomegalovirus banget mendesak;banjur amarga pangembangan terapi antiretroviral sing aktif banget, jumlah kasus sitomegalovirus mudhun banget.Amarga panjaluk pasar sing sithik, obat kasebut dirilis ing 2002 lan 2006 Penarikan ing negara-negara Uni Eropa lan AS.
(2) Macugen
Perusahaan: Dikembangake bebarengan dening Pfizer lan Eyetech.
Wektu kanggo pasar: Disetujui kanggo listing ing Amerika Serikat ing 2004.
Indikasi: Kanggo perawatan degenerasi makula sing gegandhengan karo umur neovaskular.
Cathetan: Macugen minangka obat oligonukleotida sing dimodifikasi pegylated sing bisa target lan ikatan karo faktor pertumbuhan endothelial vaskular (VEGF165 isoform), lan diwenehake kanthi injeksi intravitreal.
(3) Defitelio
Perusahaan: Dikembangake dening Jazz.
Wektu kanggo pasar: Disetujui dening Uni Eropa ing 2013, lan disetujoni dening FDA ing Maret 2016.
Indikasi: Kanggo perawatan penyakit occlusive venule hepatic sing gegandhèngan karo disfungsi ginjel utawa paru sawise transplantasi sel stem hematopoietik.
Cathetan: Defitelio minangka obat oligonukleotida, campuran oligonukleotida kanthi sifat plasmin.Iki ditarik ing 2009 amarga alasan komersial.
(4) Kinanthi
Company: Co-dikembangaké dening Ionis Pharma lan Kastle.
Wektu kanggo pasar: Disetujui ing Amerika Serikat minangka obat yatim piatu ing 2013.
Indikasi: Kanggo perawatan adjuvant hiperkolesterolemia familial homozygous.
Cathetan: Kynamro minangka obat oligonukleotida antisense, oligonukleotida antisense sing ngarahake mRNA apo B-100 manungsa.Kynamro diterbitake minangka 200 mg subcutaneously sepisan seminggu.
(5) Spinraza
Perusahaan: Dikembangake dening Ionis Pharmaceuticals.
Wektu kanggo pasar: Disetujui dening FDA ing Desember 2016.
Indikasi: Kanggo perawatan saka atrofi otot balung mburi (SMA).
Cathetan: Spinraza (nusinersen) minangka obat oligonukleotida antisense.Spinraza bisa ngganti splicing RNA saka gen SMN2 kanthi ikatan menyang situs splicing SMN2 exon 7, saéngga nambah produksi protein SMN kanthi fungsi.Ing Agustus 2016, BIOGEN Corporation nggunakake pilihan kanggo entuk hak global Spinraza.Spinraza miwiti uji klinis pisanan ing manungsa ing 2011. Mung 5 taun, disetujoni dening FDA ing 2016, nggambarake pangenalan lengkap FDA babagan khasiat.Obat kasebut disetujoni kanggo pemasaran ing China ing April 2019. Kabeh siklus persetujuan Spinraza ing China kurang saka 6 wulan.Wis 2 taun 2 sasi wiwit Spinraza pisanan disetujoni ing Amerika Serikat.Obat anyar penyakit langka manca blockbuster kuwi ing Kacepetan listing ing China wis cepet banget.Iki uga amarga "Kabar babagan Rilis Dhaptar Obat Anyar ing Luar Negeri sing Dibutuhake kanggo Riset Klinis" sing ditanggepi dening Pusat Evaluasi Narkoba tanggal 1 November 2018, sing kalebu ing kumpulan pertama 40 obat anyar asing kunci kanggo ditinjau kanthi cepet, lan Spinraza peringkat ing.
(6) Eksondys 51
Perusahaan: Dikembangake dening AVI BioPharma (mengko jeneng Sarepta Therapeutics).
Wektu kanggo pasar: Disetujui dening FDA ing September 2016.
Indikasi: Kanggo perawatan Duchenne muscular dystrophy (DMD) kanthi mutasi gen DMD ing exon 51 skipping gene.
Cathetan: Exondys 51 minangka obat oligonukleotida antisense.Oligonukleotida antisense bisa ngiket posisi exon 51 saka pre-mRNA saka gen DMD, sing nyebabake pembentukan mRNA diwasa.Eksisi, kanthi mangkono mbenerake sebagian pigura maca mRNA, mbantu pasien nyintesis sawetara bentuk dystrophin fungsional sing luwih cendhek tinimbang protein normal, saengga bisa nambah gejala pasien.
(7) Tegsedi
Perusahaan: Dikembangake dening Ionis Pharmaceuticals.
Wektu kanggo pasar: Disetujui dening Uni Eropa kanggo marketing ing Juli 2018.
Indikasi: Kanggo perawatan amiloidosis transthyretin herediter (hATTR).
Cathetan: Tegsedi minangka obat oligonukleotida antisense sing target mRNA transthyretin.Iki minangka obat sing disetujoni pisanan ing donya kanggo perawatan hATTR.Cara administrasi yaiku injeksi subkutan.Obat kasebut nyuda produksi protein ATTR kanthi nargetake mRNA transthyretin (ATTR), lan duwe rasio keuntungan-resiko sing apik ing perawatan ATTR.Ora ana tataran penyakit utawa anané kardiomiopati ora cocog.
(8) Pandhuan
Perusahaan: Dikembangake bebarengan dening Alnylam lan Sanofi.
Wektu kanggo pasar: Disetujui kanggo listing ing Amerika Serikat ing 2018.
Indikasi: Kanggo perawatan amiloidosis transthyretin herediter (hATTR).
Cathetan: Onpattro minangka obat siRNA sing nargetake transthyretin mRNA, sing nyuda produksi protein ATTR ing ati lan akumulasi celengan amiloid ing saraf perifer kanthi nargetake mRNA transthyretin (ATTR)., kanthi mangkono nambah lan nyuda gejala penyakit.
(9) Givlaari
Perusahaan: Dikembangake dening Alnylam Corporation.
Wektu kanggo pasar: Disetujui dening FDA ing November 2019.
Indikasi: Kanggo perawatan porfiria hepatik akut (AHP) ing wong diwasa.
Cathetan: Givlaari minangka obat siRNA, obat siRNA kapindho sing disetujoni kanggo marketing sawise Onpattro.Obat kasebut diwenehake kanthi subkutan lan target mRNA kanggo degradasi protein ALAS1.Perawatan Givlaari saben wulan bisa nyuda tingkat ALAS1 ing ati kanthi signifikan lan terus-terusan, saéngga nyuda tingkat neurotoksik ALA lan PBG menyang kisaran normal, saéngga nyuda gejala penyakit pasien.Data kasebut nuduhake manawa pasien sing diobati karo Givlaari nyuda 74% jumlah flare penyakit dibandhingake karo klompok plasebo.
(10) Vyondys53
Perusahaan: Dikembangaké déning Sarepta Therapeutics.
Wektu kanggo pasar: Disetujui dening FDA ing Desember 2019.
Indikasi: Kanggo perawatan pasien DMD kanthi mutasi sambatan gen dystrophin exon 53.
Cathetan: Vyondys 53 minangka obat oligonukleotida antisense.Obat oligonukleotida target proses splicing prekursor mRNA dystrophin.Ing proses ora langsung saka prekursor mRNA dystrophin, Exon 53 eksternal sebagian disambungake, yaiku ora ana ing mRNA sing wis diwasa, lan dirancang kanggo ngasilake protein dystrophin sing dipotong nanging isih fungsional, saéngga nambah kapasitas olahraga ing pasien.
(11) Waylivra
Perusahaan: Dikembangake dening Ionis Pharmaceuticals lan anak perusahaan Akcea Therapeutics.
Wektu menyang pasar: Disetujui dening Badan Obat Eropa (EMA) ing Mei 2019.
Indikasi: Minangka terapi tambahan kanggo diet sing dikontrol ing pasien diwasa kanthi sindrom chylomicronemia familial (FCS).
Cathetan: Waylivra minangka obat oligonukleotida antisense, yaiku obat pisanan sing disetujoni kanggo perawatan FCS ing donya.
(12) Lekvio
Perusahaan: Dikembangake dening Novartis.
Wektu kanggo pasar: Disetujui dening EU ing Desember 2020.
Indikasi: Kanggo perawatan hiperkolesterolemia utami diwasa (famili heterozigot lan non-famili) utawa dislipidemia campuran.
Cathetan: Leqvio minangka obat siRNA sing target PCSK9 mRNA.Iki minangka terapi siRNA penurun kolesterol (LDL-C) pisanan ing donya.Cara administrasi yaiku injeksi subkutan.Obat kasebut dianggo kanthi gangguan RNA kanggo ngedhunake tingkat protein PCSK9, sing banjur nyuda tingkat LDL-C.Data klinis nuduhake yen Leqvio bisa nyuda LDL-C kira-kira 50% ing pasien sing tingkat LDL-C ora bisa dikurangi nganti tingkat target sanajan dosis statin sing ditoleransi maksimal.
(13) Oxlumo
Perusahaan: Dikembangake dening Alnylam Pharmaceuticals.
Wektu kanggo pasar: Disetujui dening EU ing Nopember 2020.
Indikasi: Kanggo perawatan hiperoksaluria primer tipe 1 (PH1).
Cathetan: Oxlumo minangka obat siRNA sing ngarahake mRNA asam hidroksi oksidase 1 (HAO1), sing diwenehake kanthi subkutan.Obat kasebut dikembangake nggunakake teknologi konjugasi ESC-GalNAc kimia stabilisasi paling anyar saka Alnylam, sing ngidini siRNA sing diwenehake kanthi subkutan kanthi ketekunan lan khasiat sing luwih gedhe.Obat kasebut ngarahake degradasi utawa inhibisi asam hidroksi oksidase 1 (HAO1) mRNA, nyuda tingkat oksidase glikolat ing ati, lan banjur nggunakake substrat sing dibutuhake kanggo produksi oksalat lan nyuda produksi oksalat kanggo ngontrol perkembangan penyakit lan nambah gejala penyakit ing pasien.
(14) Viltepso
Perusahaan: Dikembangake dening NS Pharma, anak perusahaan saka Nippon Shinyaku.
Wektu kanggo pasar: Disetujui dening FDA ing Agustus 2020.
Indikasi: Kanggo perawatan Duchenne muscular dystrophy (DMD) kanthi mutasi gen DMD ing exon 53 skipping gene.
Cathetan: Viltepso minangka obat oligonukleotida phosphorodiamide morpholino.Obat oligonukleotida iki bisa ngiket posisi exon 53 saka pre-mRNA saka gen DMD, sing nyebabake pembentukan mRNA diwasa.Ekson dibusak sebagian, saéngga mbenerake sebagian pigura maca mRNA, mbantu pasien nyintesis sawetara bentuk dystrophin fungsional sing luwih cendhek tinimbang protein normal, saéngga bisa nambah gejala pasien.
(15) Amvuttra (vutrisiran)
Perusahaan: Dikembangake dening Alnylam Pharmaceuticals.
Wektu kanggo pasar: Disetujui dening FDA ing Juni 2022.
Indikasi: Kanggo perawatan amiloidosis transthyretin herediter diwasa kanthi polyneuropathy (hATTR-PN).
Cathetan: Amvuttra (Vutrisiran) minangka siRNA drug targeting transthyretin (ATTR) mRNA, sing diwenehake kanthi injeksi subkutan.Vutrisiran dirancang adhedhasar Alnylam kang Enhanced Stabilization Chemistry (ESC) -GalNAc platform pangiriman conjugated karo tambah potency lan metabolis stabilitas.Persetujuan terapi kasebut adhedhasar data 9 sasi saka studi klinis Tahap III (HELIOS-A), kanthi asil sakabèhé nuduhake yen terapi kasebut ningkatake gejala hATTR-PN, kanthi luwih saka 50% pasien mbalik utawa mandheg kemajuan.
4. Obat terapi gen liyane
(1) Rexin-G
Perusahaan: Dikembangake dening Epeius Biotech.
Wektu kanggo pasar: Disetujui dening Philippine Food and Drug Administration (BFAD) ing 2005.
Indikasi: Kanggo perawatan kanker lanjut sing tahan kanggo kemoterapi.
Cathetan: Rexin-G minangka injeksi nanopartikel sing diisi gen.Iki ngenalake gen mutan cyclin G1 menyang sel target liwat vektor retroviral kanggo mateni tumor padhet khusus.Cara administrasi yaiku infus intravena.Minangka obat sing ditargetake tumor sing aktif nggoleki lan ngrusak sel kanker metastatik, duwe efek tartamtu ing pasien sing ora efektif nglawan obat kanker liyane, kalebu biologi sing ditargetake.
(2) Neovasculgen
Perusahaan: Dikembangaké déning Human stem cell institute.
Wektu listing: Disetujui kanggo listing ing Rusia tanggal 7 Desember 2011, banjur kadhaptar ing Ukraina ing 2013.
Indikasi: Kanggo perawatan penyakit arteri perifer, kalebu iskemia ekstremitas abot.
Cathetan: Neovasculgen minangka terapi gen adhedhasar plasmid DNA ing ngendi gen faktor pertumbuhan endothelial vaskular (VEGF) 165 dibangun ing balung mburi plasmid lan disuntik menyang pasien.
(3) Collategene
Perusahaan: Dikembangake bebarengan dening Universitas Osaka lan perusahaan modal ventura.
Wektu listing: Disetujui dening Kementerian Kesehatan, Tenaga Kerja lan Kesejahteraan Jepang kanggo listing ing Agustus 2019.
Indikasi: Perawatan iskemia ekstremitas ngisor sing abot.
Cathetan: Collategene minangka terapi gen adhedhasar plasmid, obat terapi gen asli Jepang pisanan sing diprodhuksi dening AnGes.Komponen utama obat iki yaiku plasmid telanjang sing ngemot urutan gen faktor pertumbuhan hepatosit manungsa (HGF).Yen tamba wis nyuntikaken menyang otot saka perangan awak ngisor, ing HGF ditulis bakal ningkataké tatanan saka prau getih anyar watara prau getih occluded.Uji klinis wis dikonfirmasi efektifitas kanggo ningkatake ulkus.
END
Wektu kirim: Nov-10-2022